কোয়ান্টাম ১৪
১।
একটা পরমাণুর গায়ে লেখা থাকে তার নাম।
পড়তে হলে, ওই পরমাণুর মৌলের গ্যাস বানিয়ে তার উপর সাদা আলো মারতে হবে।
ওই আলো তারপর প্রিজম দিয়ে পাস করবে, পেছনে পর্দায় পড়বে সাত রঙের বর্ণালি।
বার্জারের কালার ব্যাঙ্ক সেখানে থাকবে কল্পনার সব রঙ, সবগুলো রঙ!
শুধু কয়েকটা বাদে।
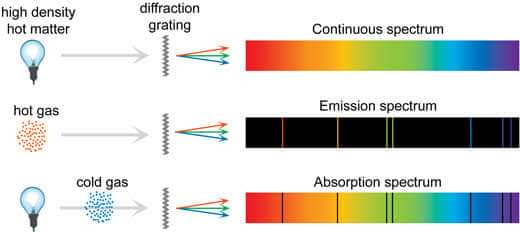
যে রঙগুলো বাদ পড়বে সেগুলো বর্ণালিতে অন্ধকার সূক্ষ্ম রেখার মতো দেখা যাবে।
কোন কোন রঙ বাদ পড়েছে, কোথায় কয়টা কালো রেখা পড়েছে দেখে বলে বলে দেওয়া যাবে মৌলের পরিচয়।
মৌল তোমার নাম কি? রঙে পরিচয়!
(এই ধরনের বর্ণালির নাম শোষণ বর্ণালি। উলটা বর্ণালিও তৈরি করা সম্ভব, যেখানে কালো ব্যাকগ্রাউন্ডে অল্প কিছু আলোর রেখা থাকবে। )
২।
বহুদিন ধরে ওই রেখাগুলো বিজ্ঞানীদের ভাবিয়েছে।
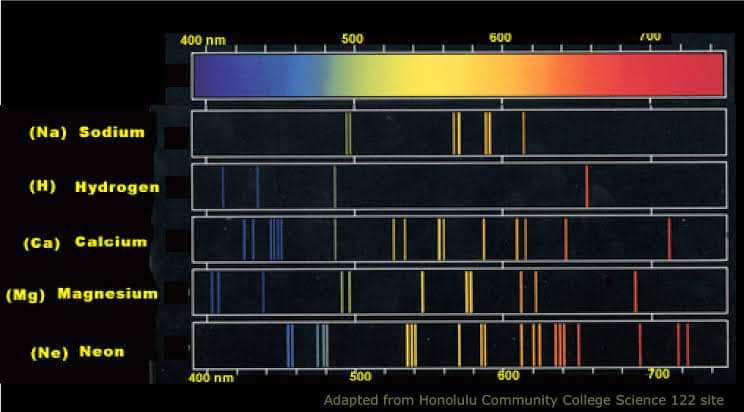
তারা জেনেছেন, প্রতিটা মৌলের জন্য আলাদা আলাদা রেখা আছে।
ওই রেখাগুলো সূর্যের বুকে হিলিয়ামের গল্প বলে।
লাল দানব তারার বুকে জ্বলন্ত কার্বনের গল্প বলে।
নববধূর গয়নায় কতটুকু সোনা, কতটুকু ভেজাল শে গল্পও তারা বলে।
কিন্তু কিভাবে বলে তারা জানতেন না।
বোর তাকিয়ে আছেন দেয়ালের ওই রংধনুর দিকে। তার চোখ আনন্দে জ্বলজ্বল করছে। ওই রেখাগুলোর রহস্য তিনি ভেদ করেছেন। প্রকৃতির ভাষা তার কাছে ফিলিপ্স বাতির মতো ক্লিয়ার হয়ে গেছে।
ওই রেখাগুলো বোরের E = hf এর গল্প বলছে।
ইলেকট্রন যখন শক্তি শোষণ করে এক স্তর থেকে অন্য স্তরে যাচ্ছে, একটা করে দাগ রেখে যাচ্ছে।
ওই দাগের কম্পাঙ্ক হবে শক্তির পার্থক্য ভাগ h.
বোর কক্ষপথগুলোর শক্তি হিসাব করেছেন। সেখান থেকে বের করে এনেছেন কোন শক্তি স্তর থেকে কোথায় গেলে কম্পাঙ্ক কি হবে। কম্পাঙ্ক জানার পর বের হয়ে আসছে তরঙ্গদৈর্ঘ্য।
প্রথম শক্তি স্তর n1, দ্বিতীয় শক্তি স্তর n2 হলে,
রেখার তরঙ্গদৈর্ঘ্য lambda হলে
1/lambda = R(1/n1^2 – 1/n2^2).
পরমাণুকে সাদা আলো খাওয়ানো হচ্ছে। ওই সাদা আলোতে সব তরঙ্গদৈর্ঘ্যের রেখা থাকে।
মনে করি, তরঙ্গদৈর্ঘ্য ১ থেকে ১০।
ওই পরমাণুর ইলেকট্রনগুলো সেখান থেকে ৪ আর ৭ তরঙ্গদৈর্ঘ্যের আলো খেয়ে উপরে উঠছে। বাকি আলো তারা ছুয়েও দেখছে না। E = hf. f না মিললে, ফালতু আলো তাদের দরকার নেই।
৪ আর ৭ খাওয়া হয়ে গেল, বাকি পড়ে থাকলো ১ ২ ৩ ৫ ৬ ৮ ৯ ১০।
ওই সংখ্যাগুলো ওই মৌলের নাম আর পরিচয়।
শুধু পরিচয়ই না, ওরা বলে, ওই মৌলের কোন কক্ষপথে কয়টা ইলেকট্রন আছে।

৩।
একের পর এক মৌল হাতে আসলো। বোর হিসাব মেলালেন। বোরের জোড়াতালি দেওয়া পরমাণুর মডেল হাইড্রোজেন ছেড়ে আরও অনেকদুর গেল।
বোর বুঝলেন, হাইড্রোজেনে আর হিলিয়ামে আছে ১টা স্তর।
লিথিয়ামে ২টা।
বোর দেখলেন, যেসব মৌলের বাইরে ৮টা করে ইলেকট্রন থাকে তারা সহজে ইলেকট্রন দিতে নিতে চায় না।
সোডিয়ামের বাইরে ১টা ইলেকট্রন আছে, ওই ইলেকট্রন ছেড়ে দিলে তার বাইরের লেয়ারে ৮টা ইলেকট্রন হবে। সোডিয়াম ওই ইলেকট্রন তাই ছেড়ে দিবে।
ক্লোরিনের দরকার একটা ইলেকট্রন। সে ওইটা গ্রহণ করবে। তারও বাইরে হবে ৮টা ইলেকট্রন।
কেন জানি সবাই ৮ সংখ্যাটা খুব পছন্দ করে!
৪।
১৯২২ সাল।
জার্মানির গটিনজেনে একটা উৎসব হলো, তার নাম বোর ফেস্টিভ্যাল।
প্রফেসর বোর পুরো পর্যায় সারণি হাতে নিয়ে আসলেন। ব্যাখ্যা করলেন কোন মৌল কিভাবে কাজ করে।
বোঝালেন কিভাবে ২ ৮ ১৮ ৩২ এর নিয়ম মেনে একের পর এক শেল পূর্ণ হয়।
বুঝালেন ঠিক কিভাবে ১টা কার্বন আর ৪টা হাইড্রোজেন মিলে মিথেন অণুর জন্ম হয়।
পর্যায় সারণিতে যে ফাঁকা জায়গা ছিল, সেখানে কে কে বসবে আর তারা কিরকম আচরণ করবে বোর নিখুঁত হিসাব দিলেন!
উপস্থিত বাঘা বাঘা প্রফেসরদের মুখ হা হয়ে গেল। কেউ প্রশ্ন করতেও ভুলে গেল, কেন এই ২ ৮ ১৮ ৩২ এর নিয়ম কাজ করে!
৫।
নিলস বোর প্রায় কোনকিছু না জেনে, বর্ণালির রেখা দেখে পুরো পর্যায় সারণির রহস্য ভেদ করে ফেলেছেন।
আজকে বোরের মডেলের ঝামেলাগুলো আর বলব না। এই জিনিয়াস মানুষটার জন্য লাল সালাম থাকলো।
১০৭ তম মৌলের নাম নিলসবোরিয়াম, প্রফেসর বোরের নামে।
(চলবে)